油滴实验(Oil-drop experiment),是罗伯特·安德鲁·密立根与其学生哈维·福莱柴尔(Harvey Fletcher)于1909年在美国芝加哥大学瑞尔森物理实验室(Ryerson Physical Laboratory)所进行的一项物理学实验,该实验首次测量出了电子的电荷量。 罗伯特·密立根因而获得1923年的诺贝尔物理学奖。
这是一个非常简单的实验,是所有大学物理的基础实验,但是这个看似简单的实验之前已经有经历很多年的积累,结合罗伯特·密立根奇思妙想才能变成里程碑式的意义。
一切还要从测量氢原子质量开始,假如知道了氢原子的质量,就能通过氢原子的质量乘以其他原子的相对原子质量,就能算出它们的真实质量了。所以接下来的问题就是我们要如何算出氢原子的质量,

有一个办法,就在19世纪的中期,这个时间比汤姆逊发现电子还早了几十年,法拉第就在电解实验中测量出来了原子的质量和单位电荷的比值,比如,氢原子的质量和单位电荷的比值就是1.044×10^-8千克/库仑。
当时法拉第并不知道这个单位电荷是啥东西,只知道这是一个在电解的过程中离子所能获得和失去的最小的单位电荷,那汤姆逊发现了电子以后,我们就知道了这就是电子所携带的电荷。每一个电子的电荷值就是单位电荷。
所以现在的关键问题又变成了电子的电荷是多少?只要求出这个值,所有的问题都可以解决,因此汤姆逊在发现电子以后,他所率领的卡文迪许实验室最重要的工作就是测量电子的电荷。

好,下面我们先说,对电子电荷的测量,后面再说法拉第的电解实验。
在说电子电荷之前,我们先了解一个东西,威尔逊云室,威尔逊是汤姆逊的学生,在卡文迪许实验室的时候,威尔逊就发现不需要尘埃颗粒,带电粒子也可以作为凝结核使得空气中的水蒸汽凝结成小水珠,这个现象的发现就意味着,我们可以借助无尘埃的过饱和水蒸汽的凝结,来显示出带电粒子的径迹。

所以威尔逊就据此发明了云室,可以让我们清楚地看到亚原子粒子的存在,这个装置为早期的粒子物理学发展做出了巨大的贡献,后来我们还发明出了很多类似的装备,比如乳胶摄影、气泡室、火花室、多丝正比室等等这些可以让粒子现身的设备。

那对电子电荷的测量,就是在云室中进行的,第一个测量的人是卡文迪许实验室的汤森,它是汤姆逊的同事,测量的基本原理是这样的,带电离子经过云室的时候会凝结成小水滴,测量这些小水滴的荷质比,然后在测量水滴的质量,就能算出离子所携带的电荷是多少了,然后根据离子的电荷就能知道电子的电荷值。
虽然带电粒子在云室中形成了水滴,但是这些水滴还是太小不能直接测量,所以要找其他的办法间接测量水滴的质量。
汤森使用的方法是测量水滴在重力的作用下下落的速度,来推算水滴的质量,这个过程其实很简单,我们知道水滴在重力的作用下会先做加速运动,随着速度的提高,空气的粘滞阻力会一直增大,直到把重力抵消掉,这个时候水滴会匀速下落。
那根据牛顿第二定律,我们就能知道水滴的重力=水滴的质量×9.8米/秒,空气的粘滞阻力,跟水滴的半径和速度成正比,在1851年的时候,斯托克斯就已经给出了粘滞阻力公式:
那作用在水滴上的粘滞阻力=6πη×水滴的半径×水滴的速度,其中η就是空气的粘滞系数,测量的值大约为1.82×10^-5牛/米。
当水滴匀速下落的时候,水滴的质量×9.8米/秒=6πη×水滴的半径×水滴匀速下落的速度。这个速度可以测量出来,所以通过这个公式就能知道水滴的质量和半径之间的关系。
水滴的质量和半径之间还有一个关系,就是水滴的质量=4π/3×水滴半径×水的密度,最后汤森就算出了云室中水滴的平均质量。
现在我们需要知道的是,云室中所有水滴的质量以及所携带的电荷是多少,汤森使用的办法是,用硫酸吸收了所有的水滴,以及其中的电荷,硫酸最终所获得的电荷以及质量都可以测出来,由于每个水滴所携带的电荷以及质量都是一样的,所以测出来的数值之比就是每个水滴的荷质比。
刚才我们已经算出了水滴的平均质量,所以汤森在1897年测量的结果是正离子的电荷值为0.9×10^-19库仑,负离子的电荷值为1×10^-19库仑,两个数据相差了10%,可以解释为实验数据的不确定性。

1898年汤姆逊也测量的电子的电荷,跟汤森使用的方法基本上一样,区别是汤姆逊云室中的离子是用X射线照射空气产生,他在测量水滴的总质量以及总电荷的时候没有用硫酸,而通过测量空气的电导率以及温度的变化,间接的测出了水滴上的荷质比,最后获得的结果是2×10^-19库仑,1901年实验经过改进,汤姆逊引用的值为1.1×10^-19库仑.
1903年,威尔逊继续跟进,也测量了电子的电荷,他测量水滴的半径和质量跟上面说的一样,都是用过测量下落速度算出来的。
区别是,威尔逊在算出水滴的质量和大小以后,就给云室施加了均匀的电场,这时水滴就受到了三个力的作用,重力、空气粘滞阻力,以及电场力。
重力可以根据刚才算出来的质量求出,粘滞阻力可以根据水滴的半径以及观测的速度算出来,电场力就等于水滴上的电荷乘以电场强度。
当这三个力再次达到平衡的时候,水滴就会匀速下落,然后我们就算出唯一一个未知量水滴的电荷,1903年威尔逊测量的值是1.03×10^-19库仑。
可以看出三个结果的一致性非常高,但是人们还是觉得这个实验有问题,总感觉误差很大,测量出来的值不准,所以到了1906年美国物理学家密里根就决定重新测量电子的电荷,他希望得到比可文迪许实验室更精确的结果。
在密里根的实验中,最大的改进就是他没有用水蒸汽,而是用了矿物油,所以叫密里根油滴实验,他用喷雾器将矿物油喷进云室当中,围绕带电离子所形成的油滴有两个特点,首先油滴表面不易蒸发,所以可以一直保证质量不变,第二个就是在水蒸汽的实验中,我们只能看到一片云雾,只能对云雾这个整体进行研究,但是矿物油就不一样了,我们可以在云室中看到单颗油滴,所以可以对它进行跟踪研究。
比如我们可以给云室施加电场,让某一颗油滴上升,然后撤掉电场,让它下降,在多次的上升和下降的过程中,我们就可以对它进行精确的测量了,最后算出它的电荷。
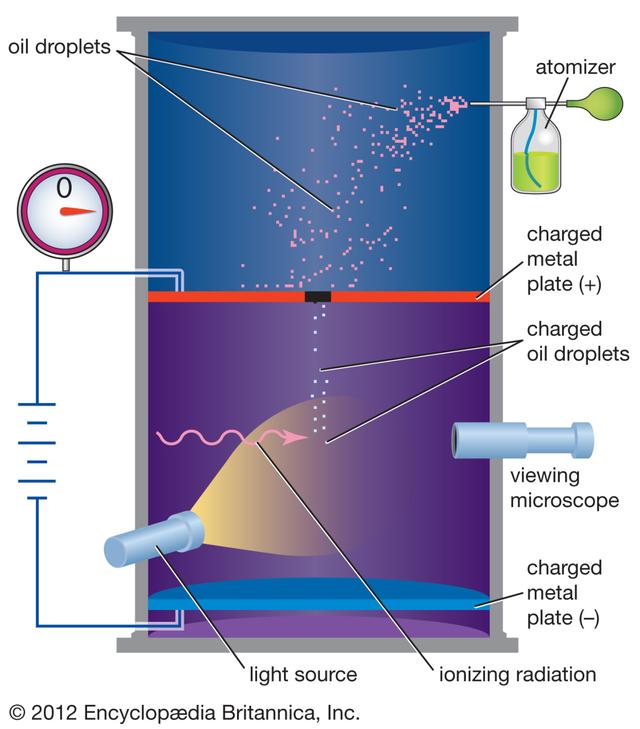
下面我们就说1911年密里根论文中的一个例子,6号油滴,在没有施加电场的时候,6号油滴在匀速下落情况下,速度为8.59×10^-4米/秒,算出来的油滴质量为8.10×10^-14千克,半径为2.76×10^-6米。
然后给油滴加上一个强度为3.18×10^5伏/米的电场,电场力的反向和重力方向相反,当油滴开始匀速上升的时候,这就说明向上的电场力和重力以及粘滞阻力的和达到了一个平衡状态。
这个时候我们又可以列出一个公式,公式中只有油滴电荷一个未知量,这里我就不写公式了,直接给出结果。通过测量向上的速度,我们就能算出这个上升油滴的电荷为29.87×10^-19库仑。
然后我们撤掉电场,让油滴下降,然后再加上电场,再次测量油滴的电荷,再撤掉电场,再加上电荷,继续测量,重复多次实验之后,我们获得了一组数据。
29.87、39.86、28.25、29.91、34.91、36.59、28.28、34.95,39.97、26.65、41.74、30.00、33.55,这些数值的单位都是10^-19库仑。
可以看出这些数字都比电子的电荷大了很多,所以这不是电子的电荷,也不是单位电荷,也很难看出他们之间有啥规律,别着急,我们先取它们之间的差值,也就是用油滴的电荷减去前一次上升时候的电荷,我们就能获得一足电荷变化的数据。
9.91、-11.61、1.66、5.00、1.68、-8.31、6.67、5.02、-13.32、15.09、-11.74、3.35,从它们差值就可以看出来,每次电荷的变化量,都是一个最小量的整数倍,可以算出这个最小的电荷大约为1.665×10^-19库仑
这个数值才是最小的单位电荷,才是电子的电荷值,这就是6号油滴测量出来的结果,那么密里根对多个油滴重复进行上述测量以后,得出来的电子电荷平均值为1.592×10^-19库仑。
这个值非常的准确,而汤森、汤姆逊和威尔逊使用水蒸汽,测量出来的电荷为整个云雾中离子电荷的平均值,所以并不准确。
好,现在我们有了电子的电荷,我们就能算出电子的质量,以及原子的质量和体积了。在这之前,我们再说下,原子的质量和单位电荷之比。
人类发现电解现象是从水开始,也是无意中看到了导线的两个极在水中可以产生氢气和氧气,那法拉第就对这个现象进行了深入的研究。
就拿水来说,现在我们知道这是因为水中有带电离子的存在,包括带正电的氢离子和带负电的氢氧根离子,当两根电极伸到水中的时候,带正电的氢离子就会被吸引到负极,然后获得两个电子,就变成了氢气,带负电氢氧根离子就跑到了正极,它们会失去四个电子,变成两个水分子和一个氧分子。
这就是电解水的过程,从这个过程中法拉第就发现, 在任意电流强度下,生成氧气的质量总是氢气质量的8倍,但是氧气的相对分子质量是氢气的16倍,这就说明,生成氢气的速率是氧气的2倍。进而法拉第就推断出生成氢气需要两个单位电荷,生成氧需要失去4个电荷电荷。跟我们现在知道的一样。
还有电解氯化银的时候,法拉第的猜测也是正确的,生成银原子需要一个单位的电荷,而生成氯气则需要2个单位的电荷。
虽然法拉第这个时候并不知道单个原子的质量,以及单位电荷是多少,但可以算出它们的比值。
比如说电解氯化银的时候,通过称量沉积阴极上的银就能知道,1安培的电流在1秒钟内可以产生10^-6千克的银。
由于一个单位的电荷就可以产生一个银原子,所以生成银原子的数目就等于1秒钟内1安培的电流所流过的单位电荷数目。
而根据定义,一安培的电流在1秒种内流过的电荷总量就是1库仑,所以说1库仑/单位电荷=10^-6千克/银原子的质量,因此银原子的质量和单位电荷的比值就是10^-6千克/库仑。
我们现在知道银原子的相对原子质量大约为氢相对原子质量的108倍,所以氢原子的质量与单位电荷之比就是10^-8千克/库仑。
还有另外一种计算方法,上回我们说的一摩尔的任何物质都具有相同的分子数,这就意味着,在电解的时候生成1摩尔的任何物质所需要的电荷量,就等于每个分子所需要的单位电荷数(比如说氢气需要2个单位的电荷、氧气需要4个)乘以法拉第常数,法拉第常数其实就是单位电荷量(单位电荷量就是电子的电荷值)乘以阿伏伽德罗常数。
比如说生成1摩尔的氢气,所需要的电荷总量就是2×法拉第常数,一摩尔的氢气重两克,所以我们就可以通过测量产生2克氢气消耗了多少电量,来算出法拉第常数。
19世纪末的时候人们测量出来的法拉第常数大约为96580库/摩,有了这个常数我们就能知道氢原子的质量和单位电荷的比值了。
我们氢的相对原子质量1.008,所以1摩尔的氢原子就重1.008克,或者是1.008×10^3千克,然后用这个数除以法拉第常数,结果就是1.044×10^-8千克/库仑,这就是氢原子的质量和单位电荷的比值。
现在密里根测出了电子的电荷值,也就是单位电荷的大小,所以我们用电子的电荷1.592×10-19库仑乘以1.044×10^-8千克/库仑,所以我们就算出了氢原子的质量为1.663×10^-27千克。
当然我们也能通过电子的质荷比算出电子的质量是9×10^-31千克。还能算出阿伏伽德罗常数,用电子的电荷值除以通过电解测量出来的法拉第常数,最后的结果是每摩尔的物质的分子数为6.062×10^23,这是密里根当年给出的结果,和今天的精确测量值相差不大。
知道了氢原子的质量,其他原子的质量都可以通过相对原子质量算出来,现在我们就估计下原子的大小,就拿金原子来说。
金原子的相对原子质量是197,所以算出来的质量是3.25×10^-25千克,金的密度是1.93×10^4千克/米,所以每立方米的金中必然有1.93×10^4/3.25×10^-25个金原子,结果是5.94×10^28个。
因此每个金原子所占的体积为1/5.94×10^28,最后结果是1.68×10^-29米,直径是2.6×10^-10米。
看到了吧,只要算出电子的电荷,最后连原子的直径都算出来了,这就是科学的魅力。太神奇了。
今天我们精确测量出来的电子电荷为1.601765×10^-19库仑,是在采用了新的空气粘滞系数以后测量出来的结果。
虽然今天我们不在测量电子的电荷值了,但目前密里根的油滴实验还在做,因为夸克模型告诉我们电子所携带的电荷并非最基本的电荷单位,质子中的两个夸克具有-2/3倍的电子电荷,1个夸克具有1/3倍的电子电荷。
所以人们希望在实验中发现这些电荷,证明夸克不仅仅是一个理论模型,而且曾经也有零星的报告说在实验中发现了具有1/3电子电荷的油滴,但这个说法没有得到广泛的确认。
